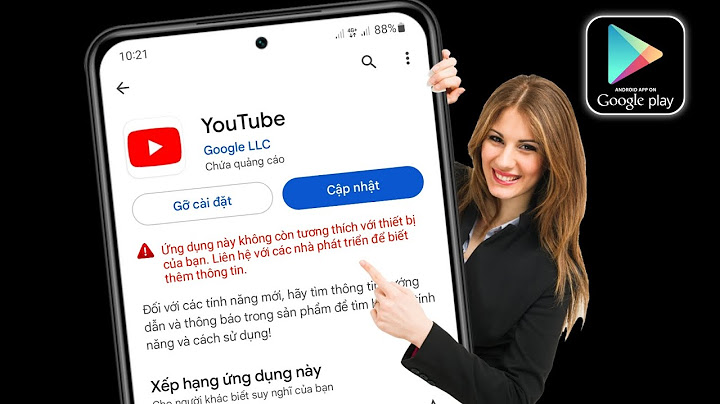
Cho hỗn hợp sản phẩm qua bình (1) đựng H2SO4 đặc, dư => H2O bị giữ lại \=> \({m_{{H_2}O}} = 0,54\,gam = > {n_{{H_2}O}} = 0,03\,mol = > {n_{H\,(trong\,X)}} = 2.{n_{{H_2}O}} = 0,06\) Cho qua bình (2) đựng KOH dư => CO2 bị giữ lại \( = > {m_{C{O_2}}} = 1,32\,gam = > {n_{C{O_2}}} = 0,03\,mol\, = > {n_C} = {n_{C{O_2}}} = 0,03\) Vì đốt cháy X chỉ thu được CO2 và H2O => X gồm C, H và có thể có O Ta có: mC + mH = 0,03.12 + 0,06 = 0,42 = mX \=> trong X không chứa O \=> nC : nH = 0,03 : 0,06 = 1 : 2 \=> CTĐGN của X là CH2 => CTPT của X có dạng (CH2)n 0,42 gam X chiếm thể tích hơi bằng thể tích của 0,192 gam O2 \=> nX = \(\frac{{0,192}}{{32}} = 0,006\,mol\) \=> MX = \(\frac{{0,42}}{{0,006}} = \,70\) => 14n = 70 => n = 5 \=> CTPT X là C5H10  DẠNG BÀI TẬP XÁC ĐỊNH CÔNG THỨC HOÁ HỌC DẠNG TOÁN : TÌM KIM LOẠI HOẶC PHI KIM Cách giải: - Gọi tên nguyên tố cần tìm là R có hoá trị là n (hoặc oxit là R20n…..) - Tính các số mol có liên quan - Lập công thức chất cần tìm hoặc viết PTHH - Lập phương trình hoặc hệ phương trình toán học ,rồi suy ra khối lượng mol nguyên tử của nguyên tố (hoặc biện luận) => nguyên tố cần tìm. Vd1: Cho 12,8 g kim loại hoá trị II phản ứng vừa đủ với clo thì thu được 27 g muối clorua. Tìm kim loại trên? Giải Gọi kim loại là R R + Cl2 → RCl2 MR gam (MR + 71)gam 12,8 gam 27 gam Ta có: 12,8. (MR + 71) = 27.MR Giải phương trình trên ta được : MR \= 64 ( Đồng : Cu) Vd2: Cho 5,4 g kim loại hoá trị không đổi phản ứng vừa đủ với dd HCl , kết thúc phản ứng thu được 6,72 lit khí (đktc). Tìm kim loại trên? Giải Gọi kim loại là R có hoá trị n ( ,n: nguyên) mol V nH3,0 4,22 72,6 4,22 2 2R + 2n HCl → 2RCln + nH2 mol 0,3mol MR \= Biện luận: n 1 2 3 MR 9 (loại) 18(loại) 27(nhận) Vậy R là nhôm (Al) Vd3: Cho 24,75g hidroxit của kim loại hoá trị không đổi tác dụng với 400d dd axit sunfuric 9,8% .Để trung hoà axit còn dư cần dung 150mldd Ca(OH)2 1M. Tìm công thức hoá học của hidroxit ? Giải Gọi công thức hoá học của hidroxit R(OH)n , n hoá trị ( ,n: nguyên) |